Membres du projet
Projet
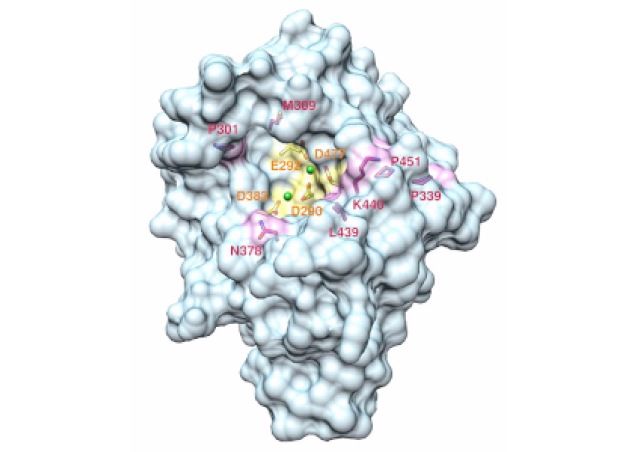
NF1 est un gène suppresseur de tumeur majeur codant la neurofibromine, une RAS-GAP (GTPase activating protein) qui agit comme un inhibiteur de la voie RAS-MAPK en permettant le retour en confirmation inactive des protéines RAS. Les altérations du gène NF1 et leur ciblage thérapeutique ont été peu étudiés dans les cancers sporadiques car il s’agit d’un long gène avec de nombreux pseudogènes et sans point chaud de mutation.
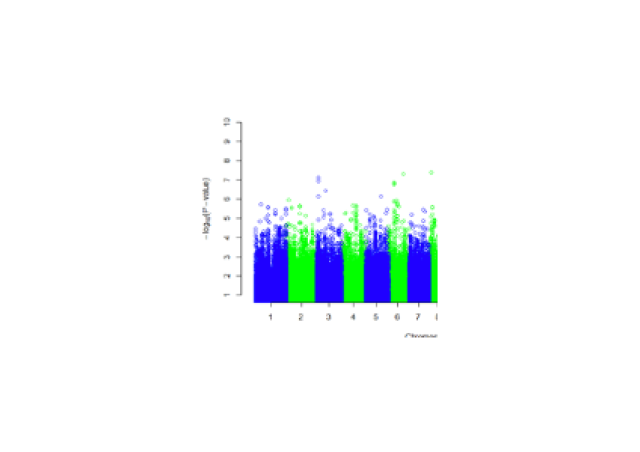
Nous avons caractérisé les altérations génétiques du gène NF1 sur une cohorte de carcinomes bronchiques non à petites cellules (CBNPC) par une approche de NGS ciblé afin de confirmer l’implication de NF1 et d’établir des corrélations génotype/phénotype. Une altération génétique de NF1 a été retrouvée dans 24/137 (17%) des échantillons de la cohorte (Tlemsani et al., 2019). Nos objectifs sont de comprendre les conséquences fonctionnelles de l’inactivation de NF1 et d’identifier de nouvelles cibles thérapeutiques potentielles des carcinomes bronchiques NF1 mutés, qui représentent donc un sous-type distinct de cancers. Nous avons développé des modèles cellulaires de carcinome bronchique muté NF1 via la technique d’édition génomique CRISPR Cas9. Notre hypothèse est que les mutations de NF1 dans le contexte de la carcinogenèse des CBNPC pourraient causer des vulnérabilités cellulaires constituant des cibles thérapeutiques par effet de létalité synthétique. Nous explorons ces létalités synthétiques avec les mutations de NF1 par des approches pharmacologiques et génétiques.
Outre les tumeurs bronchiques, notre équipe s’intéresse également à la caractérisation des mutations de NF1 et plus largement des régulateurs négatifs de la voie RAS-MAPK dans les leucémies aigues lymphoblastiques B (LAL-B) de l’enfant. En effet, l’activation des effecteurs principaux de la voie est bien décrite mais les altérations des régulateurs de cette voie sont encore actuellement mal cernées. Nous avons pour projet principal de caractériser (1) par étude transcriptomique ciblée : les variations de transcrits d’un panel de régulateurs négatifs de la voie et (2) par étude de séquençage NGS ciblé : les altérations génétiques de ces effecteurs au sein d’une grande cohorte de LAL-B pédiatriques, incluant des échantillons appariés de rechute.