Membres du projet
Projet
Seule une minorité de patients atteints de cancers solides répond aux approches d'immunothérapie. Actuellement, l’un des défis majeurs est d'identifier les mécanismes responsables de cette résistance, afin de proposer des stratégies plus efficaces pour la surmonter. Dans les cancers solides, les cellules tumorales se trouvent fréquemment dans des îlots tumoraux entourés d'un stroma composé de fibres et de cellules immunosuppressives dérivées de l'hôte. Par conséquent, afin d'éradiquer efficacement les cellules cancéreuses, les lymphocytes T (provenant de la circulation sanguine) doivent migrer activement pour traverser ce stroma et rentrer en contact avec les cellules tumorales dans les îlots tumoraux. Malheureusement, plusieurs facteurs entravent une migration intratumorale efficace des lymphocytes T, empêchant ainsi les lymphocytes T de rentrer en contact avec les cellules cancéreuses et de les tuer. Le microenvironnement hostile des cancers solides limite également l'infiltration des cellules CAR T, réduisant ainsi leur efficacité. En plus du rôle des facteurs extrinsèques (par exemple, la matrice extracellulaire et les macrophages), une migration défectueuse des lymphocytes T peut être le résultat d'une activité métabolique déficitaire. En effet, le métabolisme soutient la migration cellulaire, qui repose sur une régulation fine du remodelage du cytosquelette, pour lequel les réactions métaboliques fournissent de l'énergie sous forme d'ATP (pour l'actine) ou de GTP (pour la tubuline). Nous avons récemment caractérisé la manière dont le métabolisme régule la migration des lymphocytes T humains et nous avons identifié les principales voies métaboliques soutenant la migration des lymphocytes T infiltrant une masse tumorale solide (PMID : 38467616). Ces résultats ouvrent la possibilité de cibler le métabolisme des lymphocytes T pour améliorer leur migration intratumorale dans les tumeurs solides humaines, améliorant ainsi l'efficacité des approches actuelles d'immunothérapie. Pour atteindre cet objectif, le groupe de recherche se concentre actuellement sur les aspects suivants :
-) identification d'approches métaboliques innovantes capables d'améliorer la motilité intratumorale des cellules T et CAR T dans des modèles précliniques de tumeur solide.
-) caractérisation de la capacité migratoire des cellules T infiltrant une masse tumorale solide afin d'identifier des « signatures de motilité » qui peuvent être ciblées en thérapie.
-) analyse de l'impact de l'hétérogénéité métabolique chez les patients cancéreux sur la migration intratumorale des cellules T afin d'améliorer notre capacité à identifier les patients cancéreux avec une migration défectueuse des cellules T.
Principales technologies du laboratoire :
-) modèles in vitro 2D et 3D pour étudier la migration des cellules T
-) tranches de tumeur gardées en survie pour analyser la migration des cellules T dans un contexte tumorale
-) modèles murins précliniques de cancer solide pour l’étude de cellules CAR T
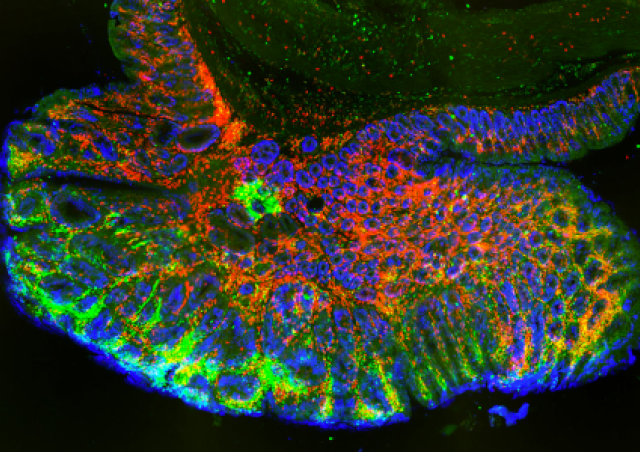
Image sur la page de l'équipe : cellules T (en vert) qui migrent dans un gel 3D de collagène. Les trajectoires sont en rouge.