Les membres du projet
Introduction
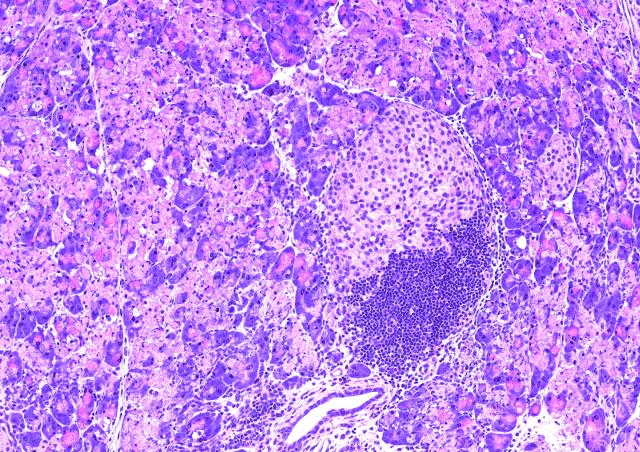
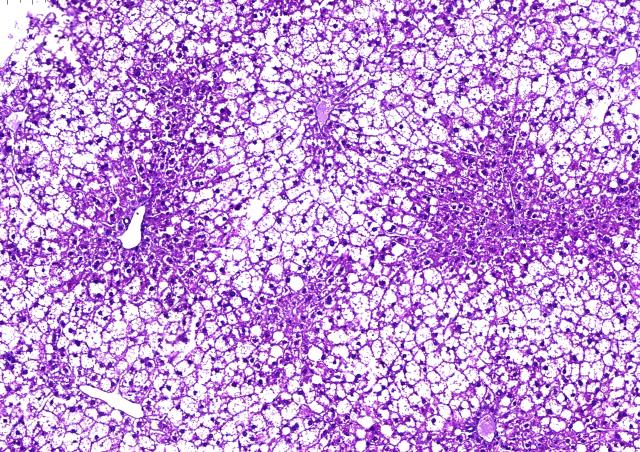
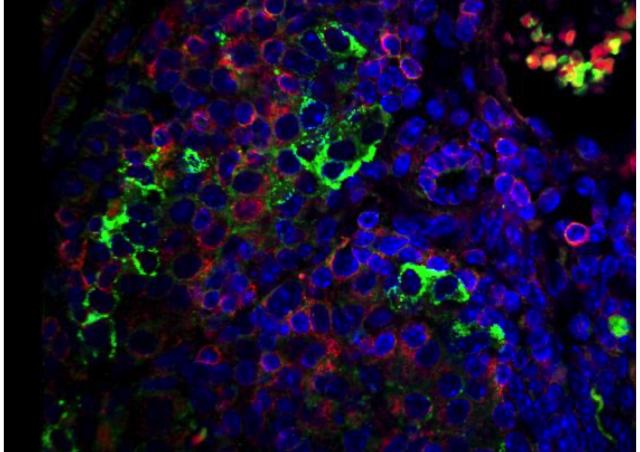
Notre principal objectif est d’identifier et d’étudier les gènes impliqués dans le diabète juvénile, allant du diabète de type 1 typique (DT1) aux formes monogéniques, dont la présentation clinique peut être atypique ou non. Le déterminisme du DT1 est multifactoriel, impliquant des facteurs génétiques et d’environnement. Les études génétiques du DT1, en particulier les études d’association pangénomiques (GWAS) menées à grande échelle, ont permis d’identifier un grand nombre de variants génétiques associés au DT1, qui n’expliquent cependant pas la totalité de la composante génétique de cette maladie. Nous faisons l’hypothèse qu’une partie de l’héritabilité manquante des diabètes pourrait être due à des formes monogéniques. Ces gènes peuvent impliquer des mécanismes multiples, immuns et non autoimmuns, affectant le développement, le fonctionnement et le maintien des cellules beta pancréatiques sécrétrices d’insuline.
Axes de recherche
Afin d’identifier et de caractériser les gènes impliqués dans la diversité des diabètes, nous avons constitué un ensemble unique de cohortes de patients et de familles, incluant des cohortes de DT1 « typique » française et internationale, et des cohortes enrichies en formes monogéniques sur différents critères de sélection. Nous utilisons des approches cliniques, génétiques et bioinformatiques ainsi que des études fonctionnelles adaptées aux gènes identifiés. Nos études de formes atypiques de diabète (diabète néonatal et diabètes syndromiques) nous ont permis d’identifier plusieurs nouveaux gènes responsables de formes monogéniques de diabètes, dont EIF2AK3, GLIS3, PPP1R15B, DUT et ONECUT1/HNF6, ainsi que la caratérisation clinique détaillée de nouvelles entités monogéniques de diabète. Nos études génétiques prennent en considération les composantes familiales et populationnelles, ce qui permet d’en augmenter la puissance. Certains de ces gènes sont partagés entre plusieurs formes de diabète, comme GLIS3 (diabète monogénique et DT1 et DT2 multifactoriels) et ONECUT1 (allant d’un diabète récessif néonatal syndromique sévère au DT2 multifactoriel). L’identification et l’étude de ces gènes apportent donc une meilleure compréhension des mécanismes impliqués dans les diabètes. Nos études ouvrent également des perspectives vers une médecine de précision/médecine personnalisée selon les risques génétiques individuels.

Publications sélectionnées
1. Delépine M, Nicolino M, Barrett T, Golamaully M, Lathrop M, Julier C. EIF2AK3, encoding translation initiation factor 2- kinase 3, is mutated in patients with Wolcott-Rallison syndrome. Nature Genetics 25: 406-409, 2000
2. Senée V, Chelala C, Duchatelet S, Feng D, Blanc H, Cossec JC, Charon C, Nicolino M, Boileau P, Cavener DR, Bougnères P, Taha D, Julier C. Mutations in GLIS3 are responsible for a rare syndrome with neonatal diabetes mellitus and congenital hypothyroidism. Nat Genet 38: 682-687, 2006
3. Zalloua P, Azar S, Delepine M, Makhoul N, Blanc H, Sanyoura M, Lavergne A, Stankov K, Lemainque A, Baz P, Julier C. WFS1 mutations are frequent monogenic causes of juvenile-onset diabetes mellitus in Lebanon. Hum Mol Genet 17:4012-4021, 2008
4. Barrett JC, Clayton D, Concannon P, Akolkar B, Cooper JD, Erlich HA, Julier C, Morahan G, Nerup J, Nierras C, Plagnol V, Pociot F, Schuilenburg H, Smyth DJ, Stevens H, Todd JA, Walker NM, Rich SS, and The Type 1 Diabetes Genetics Consortium. Genome-wide association study and meta-analysis find that over 40 loci affect risk of type 1 diabetes. Nat Genet 41, 703–707, 2009
5. Abdulkarim B*; Nicolino M*, Igoillo-Esteve M, Daures M, Romero S, Philippi A, Senée V, Lopes M, Cunha D, Harding H, Derbois C, Bendelac N, Hattersley A, Eizirik D, Ron D, Cnop M*, Julier C*. A missense mutation in PPP1R15B causes a syndrome including diabetes, short stature and microcephaly. Diabetes 64:3951-3962, 2015
6. Dos Santos RS*, Daures M*, Philippi A*, Romero S, Marselli L, Marchetti P, Senée V, Bacq D, Besse C, Baz B, Marroquí L, Ivanoff S, Masliah-Planchon J, Nicolino M, Soulier J, Socié G, Eizirik DL*, Gautier J-F*, Julier C*. dUTPase (DUT) is Mutated in a Novel Monogenic Syndrome with Diabetes and Bone Marrow Failure. Diabetes 66:1086-1096, 2017
7. Lenfant C*, Baz P*, Degavre A*, Philippi A, Senée V, Vandiedonck C, Derbois C, Nicolino M, Zalloua P, Julier C. Juvenile-onset diabetes and congenital cataract: « double-gene » mutations mimicking a syndromic diabetes presentation. Genes 8:309, 2017
8. Lytrivi M*, Senée V*, Salpea P*, Fantuzzi F*, Philippi A, Abdulkarim B, Sawatani T, Marin-Canas S, Pachera N, Degavre A, Singh P, Derbois C, Lechner D, Ladriere L, Igoillo-Esteve M, Cosentino C, Marselli L, Deleuze JF, Marchetti P, Eizirik DL, Nicolino M, Chaussenot A, Julier C*,@, Cnop M*,@. DNAJC3 deficiency induces β-cell mitochondrial apoptosis and causes syndromic young-onset diabetes. Eur J Endocrinol. 184:459-472, 2021
9. Philippi A#, Heller S#, CostaI IG#, Senée V#, Breunig M, Zhijian L, Kwon G, Illing A, Lin Q, Hohwieler M, Degavre A, Zalloua P, Liebau S, Schuster M, Krumm J, Zhang X, Geusz R, Benthuysen JR, Wang A, Goulton K, Neubauer H, Simon E, Klein T, Wagner M, Russell R, Nair G, Besse C, Olaso R, Deleuze J-F, Kuster B, Hebrok M, Seufferlein T, Sander M, Boehm BO, Oswald F, Nicolino M*, Julier C*,@, Kleger A*,@. Mutations and variants of ONECUT1 in diabetes. Nat Medicine 27:1928-1940, 2021
10. Heller S@, Melzer MK, Azoitei N, Julier C@, Kleger A@. Human Pluripotent Stem Cells Go Diabetic: A Glimpse on Monogenic Variants. Front Endocrinol 12: 648284, 2021. Review
# Equal contributions. *Equal contributions. @co-corresponding authors