L’objectif de notre équipe est de caractériser les mécanismes moléculaires contrôlant l’infection par le VIH-1. Nos projets de recherche visent plus particulièrement à définir les facteurs cellulaires proviraux qui participent à la morphogenèse du VIH-1, à identifier les barrières intrinsèques de l’hôte aux infections virales, que sont les facteurs de restriction, et à caractériser les contremesures virales à ces facteurs de restriction.
Nos travaux récents se sont focalisés sur le facteur de restriction BST2/Tétherine, barrière intrinsèque de l’hôte à la dissémination des virus enveloppés.
Nos travaux ont permis de mettre en évidence le détournement de la voie endosomale par la protéine virale Vpu pour contrer le facteur de restriction BST2/Tétherine. Nous avons également identifié la machinerie d'ubiquitination impliquée dans la régulation du trafic intracellulaire et la dégradation de BST2/Tétherine.
Nous avons réalisé la première démonstration de la contribution d'un mécanisme d'autophagie non canonique dans la contremesure virale déployée contre BST2/Tétherine. Plus récemment, nous avons caractérisé le rôle des protéines virale Vpu et cellulaire BST2/Tétherine dans la formation de sanctuaires viraux dans les macrophages.Parallèlement, nos travaux ont permis de définir d'un nouveau rôle de la protéine d'autophagie Bécline-1 dans la congression et l'alignement des chromosomes lors de la mitose.
Les avancées majeures dans le domaine de l'autophagie et la caractérisation récente par notre équipe de l'implication d'un mécanisme non canonique d'autophagie dans la levée d'une restriction virale orientent désormais nos recherches vers des projets originaux et novateurs visant à définir le rôle des fonctions non canoniques des protéines autophagiques dans le cycle réplicatif du VIH-1.
Les membres du projet
Le projet
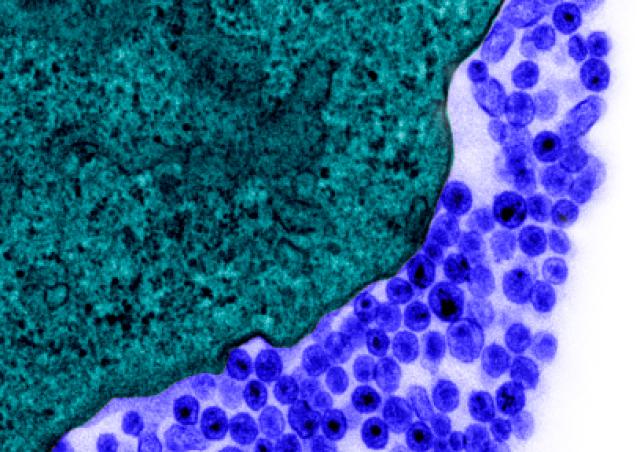
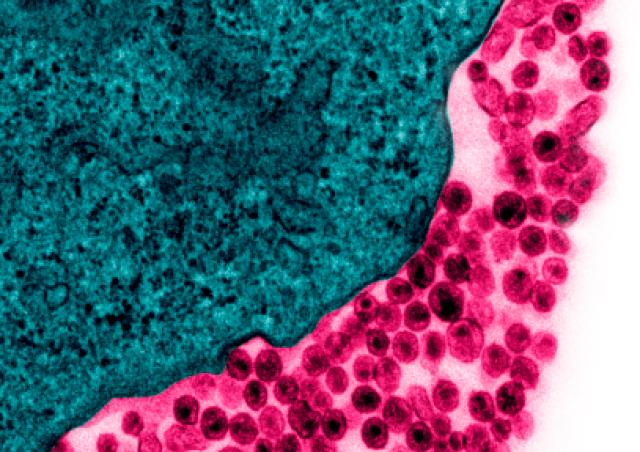
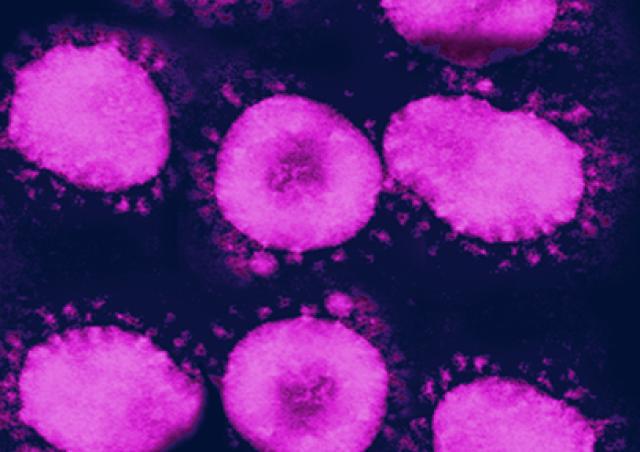
Les facteurs de restriction sont des acteurs de la réponse innée de l’hôte aux infections. Ces protéines cellulaires possèdent une activité antivirale directe. BST2 (bone marrow stromal antigen 2)/Tetherin est l’un de ces facteurs de restriction. Ce facteur réduit considérablement la libération des virus enveloppés en piégeant physiquement les particules virales matures nouvellement formées à la surface des cellules infectées. L'activité antivirale de BST2 repose sur sa présence au niveau du site de bourgeonnement viral et sur sa capacité à s'incorporer dans les virions naissants en train de bourgeonner, créant un pont entre les membranes virale et cellulaire. Les lentivirus, notamment le virus de l’immunodéficience humaine de type 1 (VIH-1) ont adopté diverses stratégies pour contrer cette restriction et ainsi optimiser leur dissémination, notamment en codant des protéines virales, comme la protéine Vpu du VIH-1.
Vpu utilise la voie d’endocytose pour contrer la restriction BST2
Nos travaux ont permis de démontrer que Vpu réduit l’expression de BST2 à la surface des cellules en perturbant son trafic intracellulaire. Vpu accélère l’adressage de BST2 vers les lysosomes, en favorisant l’ubiquitination de BST2 et son recrutement par les complexes de transport ESCRT vers la voie lysosomale. Ce ciblage préférentiel de BST2 vers la dégradation diminue de facto le recyclage et le niveau d’expression de BST2 à la membrane plasmique (Janvier et al. Plos Pathogens 2011). Nous avons également montré que cette contre-mesure virale nécessite l'intégrité de la voie d’endocytose (Caillet et al., Plos Pathogens 2011), et plus particulièrement l'activité de la GTPase Rab7A. Nous avons également défini les E3 ubiquitine ligases impliquées dans l’ubiquitination de BST2 dans un contexte physiologique ou lors d’une infection (Roy et al. J Cell Science 2017). Nos travaux soulignent l'interaction intime entre le virus et les machineries de trafic et d'endocytose de la cellule hôte (Janvier et al, Curr HIV Res. 2012 ; Roy et al., Front Microbiol. 2014).
Le détournement par Vpu d'une voie autophagique non canonique pour contrer la restriction BST2
Plus récemment, nous nous sommes intéressés à la compréhension du mécanisme moléculaire par lequel Vpu déplace BST2 du site de bourgeonnement, un processus mal compris. Cette délocalisation de BST2 du site de bourgeonnement est cruciale pour lever la restriction imposée par BST2 à la dissémination du VIH-1. Nous avons montré que le VIH-1 est capable d’engager un mécanisme semblable au processus non canonique d’autophagie de LAP (LC3-associated phagocytosis) pour contrecarrer l’activité du facteur de restriction BST2 au site de bourgeonnement. Dans ce processus, Vpu recrute la protéine d’autophagie LC3C et accélère la phagocytose des molécules de BST2 présentes au site de bourgeonnement, au sein de structures à simple membrane décorées des protéines LC3. Ce mécanisme requiert les protéines LC3C, ATG5 et Beclin-1 mais n’implique pas l’ensemble de la voie d’autophagie. Ce mécanisme de LAP-like médié par Vpu favoriserait ainsi la dissémination virale en accélérant la phagocytose des molécules de BST2 associées au virus (Madjo et Leymarie et al., Cell reports 2016).
Vpu et BST2, deux facteurs contrôlant la séquestration du VIH-1 dans les macrophages
Les macrophages sont l’une des cibles de l’infection du VIH-1. Ces cellules jouent à ce titre un rôle majeur dans la physiopathologie de l’infection en favorisant la dissémination du virus lors de contacts cellule à cellule ainsi qu’en constituant l’un des réservoirs viraux chez l’individu infecté même sous traitement antirétroviral hautement actif. Les macrophages infectés produisent également des particules virales sur une période de temps élevée et les séquestrent dans des compartiments intracellulaires spécifiques appelés VCC, issus de l’invagination de la membrane plasmique. Dans ces compartiments, les virus restent pleinement infectieux, échappent à la surveillance du système immunitaire des patients infectés et aux traitements antirétroviraux, et sont libérés ultérieurement lors des contacts cellules à cellules. Comprendre comment les particules virales sont séquestrées et persistent dans les macrophages est un enjeu majeur pour progresser dans l’éradication des sanctuaires viraux.
Très récemment, nous avons établi que Vpu et BST2 régulait la production du VIH-1 et la formation des VCC dans les macrophages. Notre étude révèle que Vpu contrôle le volume des VCC, en partie en modulant la présence de BST2 dans les VCC. Notre étude démontre également que BST2 n'est pas nécessaire à la formation des VCC (Leymarie et Lepont, J. Virol 2019). Des études sont en cours pour comprendre quels sont les facteurs cellulaires participant à la formation de ces VCC.
Perspectives
Nos travaux en cours au sein du groupe visent à identifier de nouveaux cofacteurs cellulaires, nécessaires à la dissémination du VIH-1, dans le but ultime de développer des stratégies innovantes de lutte contre le virus. Nos recherches se focalisent plus particulièrement sur la caractérisation du rôle des protéines ATG dans la réponse du VIH-1 aux facteurs de restriction et dans l'établissement d'un cycle de réplication virale productif.